Contents [非表示]
薬事・食品衛生審議会 医薬品第二部会を開催します
平成28年11月24日(木)医薬品第二部会が開催されることになりました。
今回の議題は以下の10項目
- 医薬品トレアキシン点滴静注用25mg及び同点滴静注用100mgの製造販売承認事項一部変更承認の可否及び再審査期間の指定について
- 医薬品アーウィナーゼ筋注用10000の生物由来製品及び特定生物由来製品の指定の要否、製造販売承認の可否及び再審査期間の指定並びに毒薬又は 劇薬の指定の要否について
- 医薬品キイトルーダ点滴静注20mg及び同点滴静注100mgの製造販売承認事項一部変更承認の可否及び再審査期間の指定について
- 医薬品リアメット配合錠の生物由来製品及び特定生物由来製品の指定の要否、製造販売承認の可否及び再審査期間の指定並びに毒薬又は劇薬の指定の要否について
- 医薬品デシコビ配合錠LT及び同配合錠HTの生物由来製品及び特定生物由来製品の指定の要否、製造販売承認の可否及び再審査期間の指定並びに毒薬又は劇薬の指定の要否について
- 医薬品オテズラ錠10mg、同錠20mg及び同錠30mgの生物由来製品及び特定生物由来製品の指定の要否、製造販売承認の可否及び再審査期間の指定並 びに毒薬又は劇薬の指定の要否について
- 医薬品イラリス皮下注用150mgの製造販売承認事項一部変更承認の可否及び再審査期間の指定について
- avelumabを希少疾病用医薬品として指定することの可否について
- ベバシズマブ(遺伝子組換え)を希少疾病用医薬品として指定することの可否について
- Spiramycinを希少疾病用医薬品として指定することの可否について
個人的に気になったのは以下の4つ
- キイトルーダの販売承認事項の一部変更
- リアメット配合錠
- デシコビ配合錠
- オテズラ錠
知っている薬と錠剤なら薬局でも使われるかな?という安易な考えでリストアップです。
新薬なので名前を聞いてもさっぱりわからないので、とりあえずGoogle先生に聞いてみます。
■キイトルーダは非小細胞肺がんの適応追加を今回審議するようです。
名前を聞いたことがある人も多いのではないでしょうか。
この適応追加になったらやっと薬価収載への道が見えてくるようです。
オプジーボみたいなやつっていう認識です。
11/24にオプジーボの薬価が2/1から半分になることが告示されました。キイトルーダも収載される際にはかなり薬価が低く設定されるのではないでしょうか?
厚生労働省告示第397号(11月24日)
■リアメット配合錠(Riamet)はノバルティス社の抗マラリア薬だそうです。
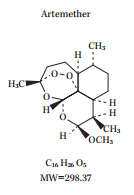
アーテメーター20mg(Artemether)とルメファントリン120mg(lumefantrine)の配合剤だそうで、欧米等60カ国以上で承認・販売されいます。
WHOガイドラインにおいて「合併症のない急性熱帯熱マラリア」の治療には、アルテミシニン誘導体と作用機序の異なる他剤を組み合わせた併用療法(ACT)第一選択薬に位置づけられています。リアメット配合錠はACTとして最も使用されている薬剤だそうです。
適応症は合併症のない急性熱帯熱マラリア
日本医療研究開発機構によると
アーテメターを含むアーテミシニン系薬のマラリア原虫に対する作用機序は明確ではない。
これらの薬剤はペルオキシド構造を有するが、ミトコンドリアでの酸化的リン酸化の阻害、取り込んだヘモグロビンからヘモゾイン生成への阻害、筋小胞体Ca ATPaseオーソログであるPf ATPase 6に対する作用などが考えられている。
ルメファントリンは、心毒性のゆえに市場から撤退したハロファントリン類似の構造を有し、キノリン化合物と同様にヘモゾイン生成の阻害が考えられている。
だそうです。
アーテメーターとルメファントリン
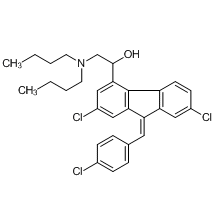
感染症法における取り扱い
マラリアは4 類感染症全数把握疾患であり、診断した医師は7 日以内に最寄りの保健所に届け出る。届出のための基準は以下の通りである。
診断した医師の判断により、症状や所見から当該疾患が疑われ、かつ、以下のいずれかの方法によって病原体診断がなされたもの。
・病原体の検出
例、血液塗抹標本による顕微鏡下でのマラリア原虫の証明と、鏡検による虫種の確認など
・病原体の遺伝子の検出
例、PCR 法など
となっています。
ノバルティス社のプレスリリースはコチラ
あまり薬局で調剤ということはなさそうなお薬でした。
■デシコビ配合錠LT及び同配合錠HT(成分:エムトリシタビン/テノホビル アラフェナミドフマル酸塩、日本たばこ産業)
「HIV-1感染症」を効能・効果とする新医療用配合薬。希少疾病用医薬品になる予定
既存抗HIV薬ツルバダの配合成分のうち、HIVの増殖に関与する逆転写酵素を阻害する作用を持つテノホビル ジソプロキシルフマル酸塩(TDF)を、テノホビル アラフェナミド(TAF)に置き換えたものだそうです。
■オテズラ錠(OTEZLA:成分:アプレミラスト)はセルジーンという会社が販売している
経口選択的ホスホジエステラーゼ4(PDE4)阻害剤です。
乾癬および乾癬性関節炎に使われる薬だそうです。
2014年3月に米FDAにより承認された治療薬で2015年時点では4億7,2000万ドル(約520億円)の売上となっていますが、 2017年には売上が14億7,300万ドル(約1,620億円)となり、 2020年には20億ドル(約2,200億円)超となるとの予想もあり、セルジーンの主要薬品のひとつになると期待されています
ただ、日本では乾癬は欧米に比べると少ないようなので、欧米程は売れないのでは?と考えられます。
薬局ではあまりお目にかかれない品目が多いようです。