Contents [非表示]
ビラノア錠20mgの特徴って何?
ビラノア錠20mg(一般名:ビラスチン)の情報が少しずつ明らかになってきています。


そこで、わかる範囲で良い点、悪い点をまとめてみました。
ビラノア錠の良い点
- 添付文書上、車の運転や機械の操作の注意書きが無い。
- 副作用の眠気の頻度も1%未満(0.6%)となっている。
- 1日1回の服用で良い。
- 卸さんの情報だと11月発売で、花粉のシーズンに間に合う。
- 禁忌は本剤過敏症のみ。
- 併用注意薬剤はエリスロマイシンとジルチアゼムのみ。
- 錠剤の大きさが直径7.0mm、厚み2.6mmとクラリチンより少し大きい(直径が0.5mm大きく、厚みは同じ)程度で飲みやすそう。
- 20mg錠のみの発売で成人には適宜増減も無い。
- 小児の適応はないものの、海外では12歳以上に使われてるらしい。
- 薬物代謝酵素(CYP)の阻害および誘導作用を有さない。
ビラノア錠の悪い点
- 食後の服用で効果が低下するようで、空腹時服用の縛りがある。
(高脂肪食の食後投与により、空腹時に比べAUC0-tが約40%、Cmaxが約60%低下したそうです) - 薬価収載から一年は14日までしか処方できない。
- 薬価は不明なものの、ザイザルより少し高いのでは?と予想される。
- 小児(15歳未満)には使えない?
- 大鵬薬品とMeiji Seikaファルマでどこまでプロモーションできるか?
効果・副作用は実際に発売になってみないと分からないですが、かなり良さそうな印象を受けます。
眠くなりにくいのは仕事をしてる人(特に運転)には非常に助かると思います

添付文書とインタビューフォームはコチラ
ビラノア錠添付文書 ビラノア錠インタビューフォーム
包装は100T、420T、500Tと欲しい包装は網羅されています。
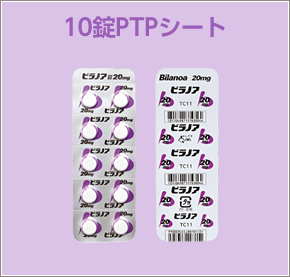
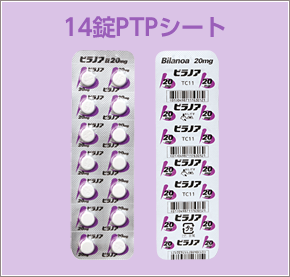
Meiji Seikaファルマ株式会社も国内共同販売契約に基づき、大鵬薬品と共同で同剤の情報提供活動および販売を行うそうです。
発売・薬価収載は11月18日 薬価は79.70円です。厚労省コード4490033F1028
発売日に早速届いた箱です。上が明治で下が大鵬

大鵬の期限の方が3か月ほど短いのですがなぜだろう???
明治のMRさんにも聞いてみたもののわからないって言われました( ̄▽ ̄;)
Meiji Seikaファルマ株式会社ホームページより引用
- 1. ビラノアは非鎮静性の経口抗ヒスタミン薬です。1)、2)
- 2. 1日1回投与で、アレルギー性鼻炎、蕁麻疹、皮膚疾患に伴うそう痒※に対して、速やかに効果を発現し、その効果は持続します。
- ●スギ花粉曝露で誘発した鼻症状を投与45分後から改善し、その効果は24時間持続しました。3)、4)
- ●通年性アレルギー性鼻炎の鼻症状を投与1日目より改善しました。5)、6)
季節性および通年性アレルギー性鼻炎の鼻症状を投与1~3日目からベースラインに比べ有意に改善し、その効果は減弱することなく季節性は4週まで、通年性は52週まで持続が確認されました。7)、8)- ●慢性蕁麻疹症状を投与1日目からプラセボと比較して有意に改善しました。9)、10)
慢性蕁麻疹および皮膚疾患に伴うそう痒※のいずれの症状も投与1~3日目からベースラインと比較して有意に改善し、その効果は減弱することなく52週まで持続が確認されました。11)- 3. 薬物代謝をほとんど受けずに未変化体のまま尿中(28.3%)および糞中(66.5%)に排泄されます。12)
また、薬物代謝酵素(CYP)の阻害および誘導作用を有しません。(in vitro)13)、14)、15)、16)- 4. 国内臨床試験において、675例中16例(2.4%)に副作用が報告されました。
主な副作用は、眠気4例(0.6%)、口渇および頭痛が各2例(0.3%)でした(承認時)。1) Farré M, et al.: Br J Clin Pharmacol., 78(5), 970( 2014)
2) Farré M: Occupation of brain histamine H-1 receptors after administration of single doses of bilastine and hydroxyzine, evaluated by positron emission tomography (PET) with [11C]-doxepin. A randomised, double-blind, cross-over clinical trialin healthy volunteers, 社内資料, 研究報告書No.697(2016)
3) スギ花粉曝露室を用いたTAC-202の前期臨床第Ⅱ相試験,社内資料, 研究報告書No.640(2016)<承認時評価資料>
4) Hashiguchi K, et al.: Allergol Int., doi:10.1016/j.alit.2016.06.009(2016)
5) 通年性アレルギー性鼻炎患者を対象としたTAC-202の臨床第Ⅲ相試験,社内資料, 研究報告書No.641(2016)<承認時評価資料>
6) Okubo K, et al.: Allergol Int., doi:10.1016/j.alit.2016.05.014(2016)
7) 通年性及び季節性アレルギー性鼻炎患者を対象としたTAC-202の臨床第Ⅲ相長期投与試験,社内資料, 研究報告書No.642(2016)<承認時評価資料>
8) Okubo K, et al:. Auris Nasus Larynx, doi:10.1016/j.anl.2016.07.021(2016)
9) 慢性蕁麻疹患者を対象としたTAC-202の臨床第Ⅱ/Ⅲ相試験,社内資料, 研究報告書No.643(2016)<承認時評価資料>
10) Hide M, et al:. Allergol Int., doi:10.1016/j.alit.2016.08.004(2016)
11) 慢性蕁麻疹及び皮膚疾患に伴うそう痒患者を対象としたTAC-202の臨床第Ⅲ相長期投与試験,社内資料, 研究報告書No.644(2016)<承認時評価資料>
12) Diaz de Rada BS: Study on the Oral Bioavailability of Bilastine, 社内資料, 研究報告書No.596(2016)
13) Johanning K: In Vitro Assessment of Human Liver Cytochrome P450 Inhibition Potential of Bilastine,社内資料, 研究報告書No.586(2016)
14) Gedey S: In vitro Interaction Studies of One Selected Test Article with MRP2(ABCC2) and BSEP(ABCB11/sPgp)ABC(efflux) Transporters, and with OATP2B1(OATP-B) and OTC1 Uptake Transporters,社内資料, 研究報告書No.588(2016)
15) Bednarczyk D: Assessment of Bilastine as an inhibitor of human NTCP, BCRP, OAT1, OAT2, OCT2, OATP1B1, and OATP1B3 mediated transport,社内資料, 研究報告書No.589(2016)
16) Johanning K: In Vitro Assessment of Cytochrome P450 Induction Potential of Bilastine in Primary Human Hepatocytes,社内資料, 研究報告書No.587(2016)
※承認された効能・効果は次の通りです。
アレルギー性鼻炎、蕁麻疹、皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒